がん医療研究部
現在研究中のテーマ

湘南鎌倉総合病院 湘南先端医学研究所 副所長
がん医療研究部 主席研究員
研究テーマ 発がん分子基盤の理解と臨床応用
研究概要
がん発生・進展制御におけるmiRNA機能本態の理解
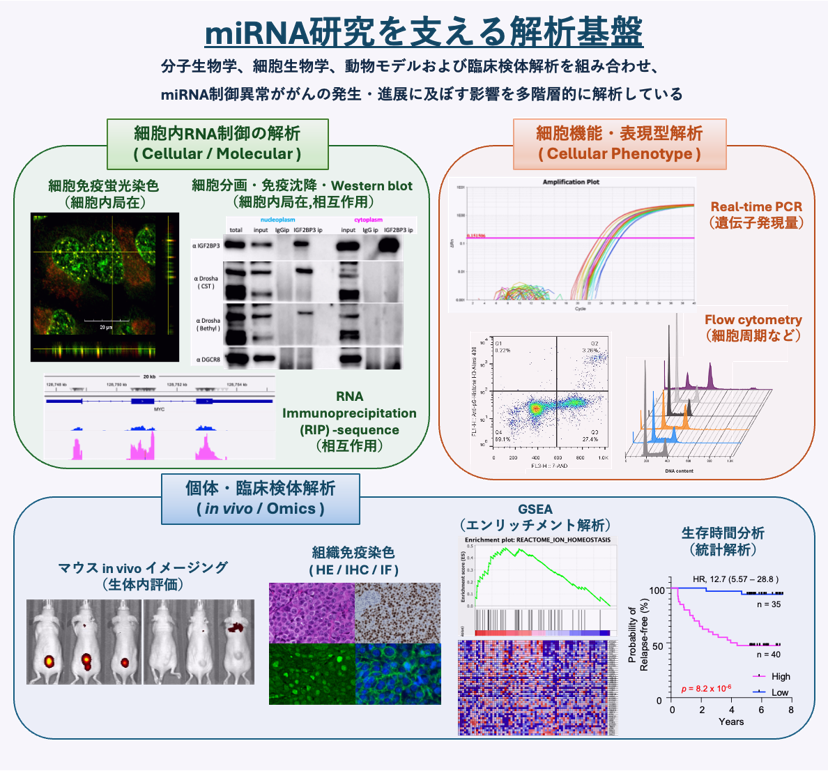
本研究室では、細胞内 non-coding RNA の一つであるマイクロRNA(microRNA; miRNA)に着目し、その機能解析を通じて発がんの分子メカニズムを理解する基礎研究を行っています。miRNA は遺伝子発現を制御する重要な因子であり、個体発生、細胞分化、細胞死といった生命現象に必須の役割を担っています。その制御異常は、がんをはじめとする多くのヒト疾患の病態形成と深く関与しています。
発がん過程では、遺伝子変異やエピゲノム異常など多層的な分子異常が生じますが、私たちは特に miRNA の発現異常や、miRNA が示す構造多様性(アイソフォーム)といった RNA レベルでの制御異常に注目して研究を進めてきました。とくに肺腺がんや大腸がんなどの固形がんにおいて、miRNA 制御機構の破綻が腫瘍の悪性化や生物学的特性の変化に深く関与することを明らかにしてきました。
近年は、胎児期に発現する RNA 結合タンパク質が miRNA の二次構造多様性を制御し、がん細胞の悪性形質を促進する新たな分子機構に着目しています。miRNA を「配列」だけでなく「構造」という観点から捉えることで、がん特異的 RNA 制御の新たな概念を提示し、がんの本質的理解につながる研究を推進しています。
基盤原理の新規診断技術・治療標的への応用
本研究室では、基礎研究で得られた知見をもとに、miRNA を用いたがんの診断・予後予測技術の開発にも取り組んでいます。特に、血清などの体液中に存在する miRNA に着目し、低侵襲でがんの特性を捉える診断基盤の構築を目指しています。
miRNA の発現量のみならず、構造多様性を含めた情報を統合的に評価することで、従来の病理学的因子や画像診断では捉えきれない腫瘍の生物学的特性や再発リスクをより精緻に層別化できる可能性が示唆されています。これにより、がんの早期診断、予後予測、さらには治療方針決定を支援する新たな分子診断技術の確立を目指しています。
基礎から臨床への橋渡しを重視し、臨床検体を用いた検証や実装を見据えた研究体制のもと、miRNA に基づく次世代のがん診断・個別化医療の実現に貢献することを目標として研究を推進しています。
代表論文・成果(Selected Publications)
- Fujiwara Y, Takahashi R, Saito M, Umakoshi M, Shimada Y, Koyama K, Yatabe Y, Watanabe S, Koyota S, Minamiya Y, Tahara H, Kono K, Shiraishi K, Kohno T, Goto A, Tsuchiya N. Oncofetal IGF2BP3-mediated control of microRNA structural diversity in the malignancy of early-stage lung adenocarcinoma. Proc Natl Acad Sci USA. 2024 Sep 3;121(36):e2407016121. doi: 10.1073/pnas.2407016121.
- Matsuzaki J, Kato K, Oono K, Tsuchiya N, Sudo K, Shimomura A, Tamura K, Shiino S, Kinoshita T, Daiko H, Wada T, Katai H, Ochiai H, Kanemitsu Y, Takamaru H, Abe S, Saito Y. Prediction of tissue-of-origin of early stage cancers using serum miRNomes. JNCI Cancer Spectr. 2023 Jan 3;7(1):pkac080. doi: 10.1093/jncics/pkac080.
- Asano N, Matsuzaki J, Ichikawa M, Kawauchi J, Takizawa S, Sakamoto H, Morioka H, Matsumoto M, Nakamura M, Yoshida A, Kobayashi E, Tanzawa Y, Kondo T, Tsuchiya N, Kawai A, Ochiya T. A serum microRNA classifier for the diagnosis of bone and soft tissue sarcomas of various histological subtypes. Nat Commun. 2019 Mar 21;10(1):1299. doi: 10.1038/s41467-019-09143-8.
- Fujiwara Y, Saito M, Robles AI, Nishida M, Takeshita F, Watanabe M, Ochiya T, Yokota J, Kohno T, Harris CC, Tsuchiya N. A nucleolar stress-specific p53-miR-101 molecular circuit functions as an intrinsic tumor-suppressor network. EBioMedicine. 2018 Jul;33:33-48. doi: 10.1016/j.ebiom.2018.06.031.
- Kurioka D, Takeshita F, Tsuta K, Sakamoto H, Watanabe S, Matsumoto K, Watanabe M, Nakagama H, Ochiya T, Yokota J, Kohno T, Tsuchiya N. NEK9-dependent proliferation of cancer cells lacking functional p53. Sci Rep. 2014 Aug 18;4:6111. doi: 10.1038/srep06111.
- Ogata-Kawata H, Izumiya M, Kurioka D, Honma Y, Yamada Y, Furuta K, Gunji T, Ohta H, Okamoto H, Sonoda H, Watanabe M, Nakagama H, Yokota J, Kohno T, Tsuchiya N. Circulating exosomal microRNAs as biomarkers of colon cancer. PLoS One. 2014 Apr 4;9(4):e92921. doi: 10.1371/journal.pone.0092921.
- Tsuchiya N, Izumiya M, Ogata-Kawata H, Okamoto K, Fujiwara Y, Nakai M, Okabe A, Schetter AJ, Bowman ED, Midorikawa Y, Sugiyama Y, Aburatani H, Harris CC, Nakagama H. Tumor suppressor miR-22 determines p53-dependent cellular fate through post-transcriptional regulation of p21. Cancer Res. 2011 Jul 1;71(13):4628-4639. doi: 10.1158/0008-5472.CAN-10-2475.
- Tsuchiya N, Nakagama H. MicroRNA, SND1, and alterations in translational regulation in colon carcinogenesis. Mutat Res. 2010 Dec 10;693(1-2):94-100. doi: 10.1016/j.mrfmmm.2010.09.001.
- Tsuchiya N, Ochiai M, Nakashima K, Ubagai T, Sugimura T, Nakagama H. SND1, a component of RNA-induced silencing complex, is up-regulated in human colon cancers and implicated in early stage colon carcinogenesis. Cancer Res. 2007 Oct 1;67(19):9568-76. doi: 10.1158/0008-5472.CAN-06-2707.
- Tazawa H, Tsuchiya N, Izumiya M, Nakagama H. Tumor-suppressive miR-34a induces senescence-like growth arrest through modulation of the E2F pathway in human colon cancer cells. Proc Natl Acad Sci USA. 2007 Sep 25;104(39):15472-15477. doi: 10.1073/pnas.0707351104.
共同研究・連携
- 国立研究開発法人 国立がん研究センター
- 国立大学法人 秋田大学
- 公立大学法人 福島県立医科大学
- 国立大学法人 東京科学大学
- 学校法人 慶應義塾 慶應義塾大学
- 国立大学法人 広島大学
- シスメックス株式会社

湘南鎌倉総合病院 湘南先端医学研究所 がん医療研究部 主席研究員
研究テーマ ハイリスク未病を規定する臓器間分子ネットワーク偏位の解明と制御戦略
研究概要
多くの疾患やQOL低下は、症状出現以前から分子・細胞レベルで進行している。我々は、将来的な機能低下へ移行するリスクを内包した状態を「ハイリスク未病」と捉え、臓器間分子ネットワークの偏位という観点からその分子基盤を解析している。筋・脳連関、翻訳制御機構、感染応答におけるエピゲノム制御に焦点を当て、ハイリスク未病の分子実態を解明するとともに、分子ネットワーク破綻を予測・層別化し、未病段階からの分子介入を可能とする先制医療の実現を目指している。
① 筋・脳連関に基づくハイリスク未病の分子基盤の解明と制御戦略
集中治療後症候群(PICS)は、高度侵襲後に未病状態を経て顕在化する代表的病態であり、筋力低下や認知機能低下が持続する。我々は重症肺障害と運動制限を組み合わせたPICSマウスモデルを確立し、骨格筋における炎症―代謝転写バランスの破綻が脳内ミクログリアの炎症優位化と神経機能低下を誘導することを示してきた。脳単一細胞RNA-seq解析では、炎症関連遺伝子高発現・ミトコンドリア関連遺伝子低発現、認知症関連モジュール活性化を特徴とするミクログリア集団を同定している。アペリン低下の関与と筋特異的補充による改善効果を明らかにするとともに、東京大学医科学研究所との共同研究により、筋由来細胞外小胞(EV)の質的変化とその機能的意義を解析している。さらに、京都大学iCeMSとの連携のもと人工転写因子(PRO-TF)を用いて炎症―代謝転写ネットワークの再同期化を試み、運動応答を分子レベルで再現する「運動模倣分子戦略(exercise mimetics)」を目指している。
加えて、ハイリスク未病の多因子性を念頭に、脳MRIのAI海馬体積自動定量基盤と徳洲会ICU縦断コホート(TMD)を統合し、分子ネットワーク偏位から脳構造変化、臨床転帰へ至る多層的連関を可視化している。これにより、ハイリスク未病の早期検出とリスク層別化、分子介入戦略の確立を目指している。(図1)

② サルコペニアにおける翻訳制御機構の解析
サルコペニアの分子基盤として、ユビキチン活性を有する翻訳制御因子CNOT4に着目している。CNOT4は翻訳抑制因子4E-BP1をユビキチン化することで筋タンパク質翻訳を維持しており、サルコペニアモデルではその発現低下が翻訳抑制を介して筋萎縮を誘導することを明らかにした。本研究は、翻訳制御層におけるネットワーク偏位という観点からサルコペニアを再定義し、分子標的介入の可能性を提示するものであり、ハイリスク未病を構成する翻訳制御層の可塑性を理解する基盤となる。
③ ウイルス感染におけるエピゲノム制御機構
インフルエンザウイルスおよびSARS-CoV-2感染において、CNOT4を介したヒストンH2Bユビキチン化が抗ウイルス遺伝子発現を制御することを明らかにした。ウイルスはこのエピゲノム制御機構を抑制することで免疫回避を図る。本研究は、感染応答におけるエピゲノム制御層の可塑性とその破綻機構を解明する試みであり、現在、京都大学iCeMSと連携してRNA修飾解析およびPRO-TFを用いた配列特異的遺伝子制御技術を発展させ、エピゲノム創薬への応用を目指している。これは、感染応答におけるエピゲノム制御層の破綻と可逆性を解明する試みである。
代表論文・成果(Selected Publications)
- Imai Y, Kimura S, Kitajima S, Sadato N, Chiba R, Hibino H, Adachi-Akahane S. Toward the promotion of “One Health” — part I: How do humans work to live together with humans, other organisms, and xenobiotics on Earth? J Physiol Sci. 2025 Nov 15;76(1):100050. doi: 10.1016/j.jphyss.2025.100050.
- Imai Y, Kinugasa Y, Nukiwa R, Llamas-Covarrubias MA, Thwin KK, Yonezaki K, Shimizu T, Yamasaki S, Shintani Y, Hashimoto H, Suzuki Y, Fujino Y, Kubodera K, Kotani T, Furuyashiki T, Penninger J, Slutsky AS. Protective Role of Apelin in a Mouse Model of Post-Intensive Care Syndrome. Am J Respir Cell Mol Biol. 2025 Sep 8. doi: 10.1165/rcmb.2025-0028OC.
- Kim MW, Yu SH, Yang U, Nukiwa R, Cho HJ, Kwon NS, Yong MJ, Kim NH, Lee SH, Lee JH, Lim JH, Kohmura Y, Ishikawa T, Henry FS, Imai Y, Oh SS, Hwang HJ, Tsuda A, Je JH. Alveolar Microdynamics during Tidal Ventilation in Live Animals Imaged by SPring-8 Synchrotron. Adv Sci (Weinh). 2024 Jul 3;11(33):e2306256. doi: 10.1002/advs.202306256.
- Kinugasa Y, Llamas-Covarrubias M, Ozaki K, Fujimura Y, Ohashi T, Fukuda K, Higashiue S, Nakamura Y, Imai Y. Post coronavirus disease 2019 syndrome in Japan: An observational study using a medical database. JMA J. 2023 Oct 16;6(4):416-425. doi: 10.31662/jmaj.2023-0048.
- Yamaguchi T, Hoshizaki M, Minato T, Nirasawa S, Asaka MN, Niiyama M, Imai M, Uda A, Chan JF, Takahashi S, An J, Saku A, Nukiwa R, Utsumi D, Kiso M, Yasuhara A, Poon VK, Chan CC, Fujino Y, Motoyama S, Nagata S, Penninger JM, Kamada H, Yuen KY, Kamitani W, Maeda K, Kawaoka Y, Yasutomi Y, Imai Y, Kuba K. ACE2-like carboxypeptidase B38-CAP protects from SARS-CoV-2-induced lung injury. Nat Commun. 2021 Nov 25;12(1):6791. doi: 10.1038/s41467-021-27097-8.
- Shiimori M, Ichida Y, Nukiwa R, Kajitani R, Fujino Y, Kikuchi A, Kawamura T, Kodama T, Toyooka S, Shirahige K, Schotta G, Kuba K, Itoh T, Imai Y. Suv4-20h2 protects from influenza virus infection through suppression of chromatin loop formation. iScience. 2021 Jun 25;24(6):102660. doi: 10.1016/j.isci.2021.102660.
- Fujiwara S, Hoshizaki M, Ichida Y, Lex D, Kuroda E, Ishii KJ, Magi S, Okada M, Takao H, Gandou M, Imai H, Hara R, Herzog H, Yoshimura A, Okamura H, Penninger JM, Slutsky AS, Uhlig S, Kuba K, Imai Y. Pulmonary phagocyte-derived NPY controls the pathology of severe influenza virus infection. Nat Microbiol. 2019 Feb;4(2):258-268. doi: 10.1038/s41564-018-0289-1.
- Morita M, Kuba K, Ichikawa A, Nakayama M, Katahira J, Iwamoto R, Watanebe T, Sakabe S, Daidoji T, Nakamura S, Kadowaki A, Ohto T, Nakanishi H, Taguchi R, Nakaya T, Murakami M, Yoneda Y, Arai H, Kawaoka Y, Penninger JM, Arita M, Imai Y. The lipid mediator protectin D1 inhibits influenza virus replication and improves severe influenza. Cell. 2013 Mar 28;153(1):112-25. doi: 10.1016/j.cell.2013.02.027.
- Imai Y, Kuba K, Neely GG, Yaghubian-Malhami R, Perkmann T, van Loo G, Ermolaeva M, Veldhuizen R, Leung YH, Wang H, Liu H, Sun Y, Pasparakis M, Kopf M, Mech C, Bavari S, Peiris JS, Slutsky AS, Akira S, Hultqvist M, Holmdahl R, Nicholls J, Jiang C, Binder CJ, Penninger JM. Identification of oxidative stress and Toll-like receptor 4 signaling as a key pathway of acute lung injury. Cell. 2008 Apr 18;133(2):235-49. doi: 10.1016/j.cell.2008.02.043.
- Imai Y, Kuba K, Rao S, Huan Y, Guo F, Guan B, Yang P, Sarao R, Wada T, Leong-Poi H, Crackower MA, Fukamizu A, Hui CC, Hein L, Uhlig S, Slutsky AS, Jiang C, Penninger JM. Angiotensin-converting enzyme 2 protects from severe acute lung failure. Nature. 2005 Jul 7;436(7047):112-6. doi: 10.1038/nature03712.
共同研究・連携
-
- 徳洲会ICU縦断コホートおよび徳洲会医療データベース(TMD)
- 湘南先端医学研究所(ヒト脳MRI AI海馬体積定量)
- 東京大学医科学研究所(EV解析)
- 京都大学 iCeMS(人工転写因子・RNA修飾研究)
- システムバイオロジー機構(マルチモーダルデータ統合解析

湘南鎌倉総合病院 湘南先端医学研究所 がん医療研究部 主席研究員
一般社団法人徳洲会グループ オンコロジープロジェクト 特別顧問
社会福祉法人湘南愛心会 介護老人保健施設かまくら 施設長
研究テーマ KRAS、BRAF癌の治療薬の開発”と“組織再生機構の解明”
がん医療研究部ニュース
-
-
-
2022年2月新津洋司郎の論文「MAPKシグナルに於けるGlutathione-s Transferase P1のCRAFシャペロン蛋白としての意義ーDr.Irving Listowskyを追悼して」が日本学士院の雑誌に掲載されました。
-
2021年11月新津洋司郎が今までの功績が認められ瑞宝中綬章しました。
同章は、公共的な職務の複雑度。困難度、責任の程度などを氷解し、重要と認められる職務を果たし、成績を上げた人物に授与される勲章で、長年進めてきた多岐に渡る医学研究の成果が評価されました。
-
2021年8月新津洋司郎が日経バイオテクにて「グルタチオンS-転移酵素P型(GSTP)1とKRASとの相互作用を選択的に阻害する薬剤の研究について」取材を受けました。
-
2020年8月新津洋司郎の論文「A CRAF/glutathione-S-tansferase P1 complex sustains autocrine growth of cancers with KRAS and BRAF mutations」が米誌『米国科学アカデミー紀要(PNAS)』に掲載されました。
-
-
スタッフ紹介

湘南鎌倉総合病院 湘南先端医学研究所 がん医療研究部 部長・主席研究員
| 略歴 | 1982年 筑波大学医学専門学群卒業 1982-1984年 筑波大学病理レジデント 1984-1987年 国立がんセンター研究所、リサーチレジデント 1987-1992年 国立がんセンター研究所病理部研究員 1992-1996年 国立がんセンター研究所第3組織病理研究室、室長 1989-1990年 国立がん研究所(NCI, Laboratory of Human Carcinogenesis)(米国) 1996-2004年 筑波大学基礎医学系・教授 2004-2011年 筑波大学人間総合科学研究科・教授 2011-2022年 筑波大学医学医療系・教授 2022年-現在 湘南先端医学研究所・主席研究員、成田富里徳州会病院・病理部長 |
|---|---|
| 受賞歴 | 2009年 国際肺癌学会 Mary J. Matthew’s award 2015年 日本病理学賞(宿題報告) 2017年 Best Faculty Member (筑波大学) |
| 専門領域 | 人体病理学 肺癌の発生と悪性化 |

湘南鎌倉総合病院 湘南先端医学研究所 副所長
がん医療研究部 主席研究員
| 略歴 | 1998年3月 横浜市立大学大学院総合理学研究科自然システム専攻修了(理学博士) 1998年4月 国立がんセンター研究所・生化学部リサーチレジデント 1998年11月 国立がんセンター研究所・生化学部・研究員 2008年3月 同・担がん生体研究室長 2013年7月 国立研究開発法人国立がん研究センター・研究所ゲノム生物学研究分野・ユニット長 2017年4月 同・研究所・分子発がん研究ユニット・独立ユニット長 2025年10月 医療法人徳洲会湘南鎌倉総合病院・湘南先端医学研究所 国立がん研究センター研究所・ゲノム生物学研究分野・客員研究員 |
|---|---|
| 所属学会と活動 | 日本癌学会 日本分子生物学会 米国癌学会 日本細胞小胞学会 Japanese Journal of Clinical Oncology reviewer board member Carcinogenesis Editorial Board Member |
| 専門領域 | がん生物学 分子細胞生物学 |

湘南鎌倉総合病院 湘南先端医学研究所 がん医療研究部 主席研究員
| 略歴 |
1985年 昭和大学医学部卒業、医師免許取得 |
|---|---|
| 受賞歴 |
日本薬理学会 江橋節郎賞 |

医学博士
湘南鎌倉総合病院 湘南先端医学研究所 がん医療研究部 主席研究員
一般社団法人徳洲会グループ オンコロジープロジェクト 特別顧問
社会福祉法人湘南愛心会 介護老人保健施設かまくら 施設長
| 略歴 |
1968年 札幌医科大学 卒業 |
|---|---|
| 受賞歴 |
1977年 日本電気泳動学会賞 |





